|
Органическая химия. Вопросы.
|
|
| Egor | Дата: Воскресенье, 15.06.2014, 22:08 | Сообщение # 1 |
|
Группа: Пользователи
Сообщений: 267
| Возьмем альдегид и восстановим его LiAlH4.
Что будет в продуктах? Спирт, понятно, а что от алюмогидрида "останется"?
|
|
| |
| |
| |
| FilIgor | Дата: Воскресенье, 15.06.2014, 22:10 | Сообщение # 2 |
 Эксперт
Группа: Супермодераторы
Сообщений: 6490
| Гидроксиды, что там еще может остаться.
Если восстановление идет в кислой среде - соли.
|
|
|
It's futile to speculate about what might have been |
| |
| |
| Ефим | Дата: Воскресенье, 15.06.2014, 22:29 | Сообщение # 3 |

Группа: Супермодераторы
Сообщений: 1839
| Да, после разложения РМ - гидроксиды (соли). А до того - комплексный алкоголят:
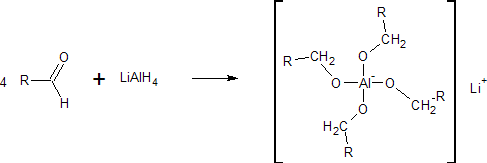
Эмм... дабы предупредить вопрос - минус на алюминии - это условность, минус там раскидан по кислородам 
Сообщение отредактировал Ефим - Воскресенье, 15.06.2014, 22:32 |
|
| |
| |
| |
| Egor | Дата: Четверг, 26.06.2014, 14:19 | Сообщение # 4 |
|
Группа: Пользователи
Сообщений: 267
| Спасибо.
Сейчас на практике выполняем самостоятельную работу.
Частью ее является определение стерильности/фертильности пыльцы.
Берем пыльцевые зерна, капаем ацетокармин, греем, смотрим в микроскоп.
Гуглил, гуглил, не нашел структурную формулу ацетокармина.
Можете нарисовать? Очень поможет.
|
|
| |
| |
| |
| Ефим | Дата: Четверг, 26.06.2014, 17:45 | Сообщение # 5 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Гуглил, гуглил, не нашел структурную формулу ацетокармина. Можете нарисовать? Очень поможет.
Ацетокармин получается из кармина растворением в большом избытке 45%-й уксусной кислоты. Это или просто раствор, или там какой-то из гидроксилов ацетилируется, или идёт ацетилирование в ядро (там есть одно свободное местечко). С красителями, особенно такими специальными, часто так - биологам формула неинтересна, а у химиков руки не доходят - разобраться 
|
|
| |
| |
| |
| Egor | Дата: Четверг, 21.08.2014, 17:01 | Сообщение # 6 |
|
Группа: Пользователи
Сообщений: 267
| Помогите, пожалуйста, с таким вопросом разобраться.
Учитывая механизм галогенирования алканов, объясните, почему кислород подавляет хлорирование (кислород в основном состоянии представляет собой бирадикал -О-О-).
|
|
| |
| |
| |
| Ефим | Дата: Четверг, 21.08.2014, 20:37 | Сообщение # 7 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Учитывая механизм галогенирования алканов, объясните, почему кислород подавляет хлорирование (кислород в основном состоянии представляет собой бирадикал -О-О-).
Фотохимическое хлорирование углеводородов - цепная радикальная реакция. В стадии переноса цепи участвуют радикалы Cl*. В присутствии кислорода проходит реакция
Cl* + O2 ----> [Cl-O-O-] ----> ClO2
Образующийся оксид хлора намного менее активен, и на нём реакция хлорирования обрывается. Так как длина цепи составляет сотни тысяч актов, даже небольшая примесь кислорода сильно тормозит реакцию.
Кнорре, Крылова, Музыкантов "Физическая химия"
Тут стоит отметить, что сам оксид хлора может дать начало новой цепи под воздействием УФ-кванта, но в любом случае средняя длина цепи в присутствии кислорода уменьшается, что проявляется в уменьшении скорости реакции.
|
|
| |
| |
| |
| Egor | Дата: Четверг, 21.08.2014, 23:37 | Сообщение # 8 |
|
Группа: Пользователи
Сообщений: 267
| Понял. Большое спасибо!
Помогите, пожалуйста, с последним вопросом разобраться.
Почему каталитическое количество тетраэтилсвинца ускоряет галогенирование метана (энергия связи Pb-C2H5 очень мала, составляет 31 ккал/моль)?
|
|
| |
| |
| |
| Ефим | Дата: Пятница, 22.08.2014, 23:19 | Сообщение # 9 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Почему каталитическое количество тетраэтилсвинца ускоряет галогенирование метана (энергия связи Pb-C2H5 очень мала, составляет 31 ккал/моль)?
При распаде ТЭС (фотохимически, или при нагревании) образуется высокоэнергичный этильный радикал (С2H5*), который инициирует цепную реакцию замещения. А поскольку связь С-Pb куда менее прочная, чем связь Cl-Cl, то и эффективность инициирования выше.
Вопрос, вообще - не такой простой, ибо ТЭС катализирует хлорирование ЭТАНА намного эффективнее, чем метана. Настолько эффективно, что даже из природного газа (90% метана, 10% этана) можно селективно получать хлорэтан.
Тут ещё другое интересно - тот же ТЭС ударно ИНГИБИРУЕТ реакцию цепного окисления углеводородов при высокой температуре. Навскидку я нашёл описание "перекисной теории" этого ингибирования - антидетонаторы, но какая-то она кривая, на мой вкус 
|
|
| |
| |
| |
| денис1 | Дата: Пятница, 29.08.2014, 20:14 | Сообщение # 10 |

Группа: Пользователи
Сообщений: 1146
| Кислород - бирадикал, возможна ли полимеризация кислорода хотя бы до O4? Предполагаю, что такие соединения будут крайне термодинамически нестабильны, вероятно, будут существовать только при очень низких температурах. У кислорода свободные электроны на разрыхляющих МО, поэтому димеризация будет невыгодна, но то же самое наблюдается для NO, который может димеризоваться, хотя и в незначительной степени.
|
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |
| Ефим | Дата: Пятница, 29.08.2014, 20:23 | Сообщение # 11 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата денис1 (  ) Кислород - бирадикал, возможна ли полимеризация кислорода хотя бы до O4? Предполагаю, что такие соединения будут крайне термодинамически нестабильны, вероятно, будут существовать только при очень низких температурах. У кислорода свободные электроны на разрыхляющих МО, поэтому димеризация будет невыгодна, но то же самое наблюдается для NO, который может димеризоваться, хотя и в незначительной степени.
Где-то я читал про О4 (не у Некрасова ли?), который в жидком кислороде существует. Надо будет посмотреть.
|
|
| |
| |
| |
| денис1 | Дата: Пятница, 29.08.2014, 21:39 | Сообщение # 12 |

Группа: Пользователи
Сообщений: 1146
| Погуглил.
Журнал "Химия и химики":
В 2001, было проведено исследование структуры свободных молекул О4[короткоживущая частица] методом
усовершенствованной масс-спектроскопии. Полученные данные не согласуются ни с
одной из ранее предсказанных структур. Результаты работы свидетельствуют об
образовании комплекса между двумя молекулами O2, одна из которых находится в
основном, другая – в специфическом возбужденном состоянии.
Однако современные расчеты показали, что хоть в жидком кислороде и отсутствуют
стабильные молекулы О4, существует тенденция ассоциации двух молекул О2 с
антипараллельными спинами.
Также есть такое заявление в каком-то реферате:
Имеется еще одна модификация кислорода - четырехатомная (О4)
Эта модификация образуется при слабом взаимодействии двух молекул кислорода. Содержание четырехатомных молекул в газообразном кислороде в обычных условиях составляет всего лишь 0,1% от общего числа молекул, в жидком и твердом кислороде — до 50%. Существует равновесие:
2О2 — О4
При низких температурах оно смещено вправо, т. е. в сторону образования молекул О4. Структурные изменения молекул вызывают различия в свойствах веществ. Так, жидкий и твердый кислород в отличие от газообразного окрашены в синий цвет.
Слишком как-то противоречиво. Ефим, что думаете?
|
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |
| Ефим | Дата: Пятница, 29.08.2014, 23:20 | Сообщение # 13 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата денис1 (  ) Имеется еще одна модификация кислорода - четырехатомная (О4) Эта модификация образуется при слабом взаимодействии двух молекул кислорода. Содержание четырехатомных молекул в газообразном кислороде в обычных условиях составляет всего лишь 0,1% от общего числа молекул, в жидком и твердом кислороде — до 50%. Существует равновесие:
2О2 — О4
При низких температурах оно смещено вправо, т. е. в сторону образования молекул О4. Структурные изменения молекул вызывают различия в свойствах веществ. Так, жидкий и твердый кислород в отличие от газообразного окрашены в синий цвет.
Вот это я и имел в виду.
Цитата денис1 (  ) В 2001, было проведено исследование структуры свободных молекул О4[короткоживущая частица] методом усовершенствованной масс-спектроскопии. Полученные данные не согласуются ни с
одной из ранее предсказанных структур. Результаты работы свидетельствуют об
образовании комплекса между двумя молекулами O2, одна из которых находится в
основном, другая – в специфическом возбужденном состоянии.
Однако современные расчеты показали, что хоть в жидком кислороде и отсутствуют
стабильные молекулы О4, существует тенденция ассоциации двух молекул О2 с
антипараллельными спинами.
Как-то всё расплывчато. "Современные расчёты" - а как спектральные данные, что в рентгене твёрдого кислорода? Посчитали, что "стабильных молекул нет" но "существует тенденция к ассоциации". Какой-то бюрократический воляпюк - много слов и ничего не сказано.
Тут слишком мало информации. Двумя статьями такие вопросы не решаются.
|
|
| |
| |
| |
| денис1 | Дата: Суббота, 30.08.2014, 01:39 | Сообщение # 14 |

Группа: Пользователи
Сообщений: 1146
| Цитата Ефим (  ) Тут слишком мало информации. |
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |
| денис1 | Дата: Суббота, 30.08.2014, 15:33 | Сообщение # 15 |

Группа: Пользователи
Сообщений: 1146
| Посмотрел. Ни слова об O4 ни в Некрасове, ни в Гринвуде, Эрншо.
Ефим, Вы нашли что-нибудь об этом неуловимом соединении?
|
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |