|
Органическая химия. Вопросы.
|
|
| Egor | Дата: Воскресенье, 21.12.2014, 22:17 | Сообщение # 271 |
|
Группа: Пользователи
Сообщений: 267
| Спасибо!
Как можно рационально получить аллил-циклогексиловый эфир?
С6H11ONa + Cl-CH2-CH=CH2 ---> эфир.
Так ведь можно, по Вильямсону?
|
|
| |
| |
| |
| Ефим | Дата: Воскресенье, 21.12.2014, 22:27 | Сообщение # 272 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Нагревание какого простого эфира с HBr даёт единственное бромпроизводное? а) любой простой эфир
б) любой симметричный эфир
в) любой метиловый эфир
г) любой циклический эфир
д) любой алкилариловый эфир
Какой(ие) продукт(ы) образуются в этой реакции с тетрагидрофураном?
Очевидно, что единственное бромпроизводное образуется из любого симметричного эфира (просто от безысходности  ). ).
Метиловые эфиры могут двояко расщепляться. Если второй радикал - первичный или вторичный алкил, то расщепление идёт в основном по Sn2 механизму с образованием метилбромида. Атакуется менее стерически загруженный атом углерода метильной группы. А вот в случае третичного, или бензильного радикала реализуется Sn1 механизм и бром уходит к этому радикалу.
Циклический эфир может оказаться несимметричным, но центр такой "диссимметрии" может быть удалён от реакционного центра, в результате чего будут получаться два продукта (хоть и в разном количестве). Скажем, такой эфир как 4-метилоксациклоооктан:
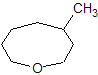
при расщеплении даст два разных бромпроизводных в практически равных количествах.
Алкилариловые эфиры расщепляются всегда с образованием бромалкила и соответствующего фенола.
Стало быть ответ - б),д)
С тетрагидрофураном получится 4-бромбутанол-1.
Сообщение отредактировал Ефим - Воскресенье, 21.12.2014, 22:28 |
|
| |
| |
| |
| Egor | Дата: Воскресенье, 21.12.2014, 22:58 | Сообщение # 273 |
|
Группа: Пользователи
Сообщений: 267
| Спасибо!
Я думал, что из симметричного, но стеснялся 
У нас есть бромбензол, реактивы Гриньяра и другая органика, нужно получить 2-фенилэтанол. Рационально получить.
Мы получим бензальдегид, потом подействуем реактивом Гриньяра и получим вторичный спирт. А нужен первичный. Как быть, подскажите, пожалуйста.
|
|
| |
| |
| |
| Ефим | Дата: Воскресенье, 21.12.2014, 23:35 | Сообщение # 274 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) У нас есть бромбензол, реактивы Гриньяра и другая органика, нужно получить 2-фенилэтанол. Рационально получить. Мы получим бензальдегид, потом подействуем реактивом Гриньяра и получим вторичный спирт. А нужен первичный. Как быть, подскажите, пожалуйста.
Если есть другая органика, то реактив Гриньяра надо из бромбензола получить. А потом ввести его в реакцию с окисью этилена. Окись этилена - продукт "большой химии", куда уж рациональнее.
Впрочем, если такой вариант не нравится - можно ещё подумать, но - завтра. Ибо поздно, а на службу надо 
|
|
| |
| |
| |
| Egor | Дата: Вторник, 13.01.2015, 23:23 | Сообщение # 275 |
|
Группа: Пользователи
Сообщений: 267
| Сказали, что нуклеофил может быть одновременно и нуклеофугом.
Можете какой-нибудь пример реакции такой привести?
Я пока не сообразил
|
|
| |
| |
| |
| Ефим | Дата: Среда, 14.01.2015, 00:00 | Сообщение # 276 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Сказали, что нуклеофил может быть одновременно и нуклеофугом. Можете какой-нибудь пример реакции такой привести?
Я пока не сообразил
При описании нуклеофильного замещения вводится такое понятие, как "хорошая уходящая группа". Ей приписывается свойство "нуклеофобности". Есть два вида "хороших уходящих групп". Это - частицы, стабильные сами по себе. не несущие заряда (вода, HOR), или анионы с распределённым зарядом (трудно поляризуемые), не требующие существенной сольватации при образовании (гидросульфат, сульфонат, фторсульфонат, нитрат и прочие того же рода). Такие группы - слабые или вообще никакие нуклеофилы.
Другой вид - это легко поляризуемые анионы, которые стабильны в хорошем растворителе. Это, например - анионы галогенов (за исключением фтора). Хлорид, бромид, иодид анионы - хорошие уходящие группы (то бишь - нуклеофобы). Но с другой стороны - они же и хорошие нуклеофилы.
|
|
| |
| |
| |
| Grey | Дата: Понедельник, 19.01.2015, 20:16 | Сообщение # 277 |
|
Группа: Пользователи
Сообщений: 133
| Доброго времени суток!
Возник вопрос при рассмотрении механизма сульфохлорирования алканов, точнее замечание к нему. В учебнике под редакцией Травеня говорится, что замещение у третичных атомов углерода не происходит, из-за пространственных затруднений, в других учебниках (А.Терней, О.А.Реутова и др., А.Н.Несмеянова) об этом ничего не говорится, поиск в интернете также не дал какого-либо ответа.
Хотелось бы узнать, происходить замещение или нет?
|
|
| |
| |
| |
| Ефим | Дата: Понедельник, 19.01.2015, 21:18 | Сообщение # 278 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Grey (  ) Хотелось бы узнать, происходить замещение или нет?
Травень тут не ошибается. Ф. Азингер ("Химия и технология парафиновых углеводородов") пишет: "третичный углеводородный атом не сульфохлорируется". Так же у Вульфсона ("Препаративная органическая химия") указано, что из изобутана получается только первичный сульфохлорид.
Кстати, этой инфой я обязан гуглю. ТщательнЕе надо искать, тщательнЕе! 
|
|
| |
| |
| |
| FilIgor | Дата: Понедельник, 19.01.2015, 21:22 | Сообщение # 279 |
 Эксперт
Группа: Супермодераторы
Сообщений: 6490
| Цитата Ефим (  ) ТщательнЕе надо искать, тщательнЕе!
Прочел фразу - возникло ощущение, что чего-то не хватает.
ТщательнЕе надо искать, товарищи, тщательнЕе!
Кажись, полегчало.
|
|
|
It's futile to speculate about what might have been |
| |
| |
| Ефим | Дата: Понедельник, 19.01.2015, 21:53 | Сообщение # 280 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата FilIgor (  ) Кажись, полегчало

|
|
| |
| |
| |
| Grey | Дата: Вторник, 20.01.2015, 18:48 | Сообщение # 281 |
|
Группа: Пользователи
Сообщений: 133
| Цитата Ефим (  ) Травень тут не ошибается. Ф. Азингер ("Химия и технология парафиновых углеводородов") пишет: "третичный углеводородный атом не сульфохлорируется". Так же у Вульфсона ("Препаративная органическая химия") указано, что из изобутана получается только первичный сульфохлорид. Кстати, этой инфой я обязан гуглю. ТщательнЕе надо искать, тщательнЕе!
Цитата FilIgor (  ) Прочел фразу - возникло ощущение, что чего-то не хватает. ТщательнЕе надо искать, товарищи, тщательнЕе!
Кажись, полегчало 
|
|
| |
| |
| |
| Egor | Дата: Среда, 21.01.2015, 23:26 | Сообщение # 282 |
|
Группа: Пользователи
Сообщений: 267
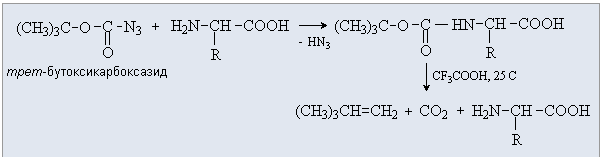
| Есть у нас Бок-защита.
Что есть HN3 ? Я с таким не сталкивался...
|
|
| |
| |
| |
| Ефим | Дата: Среда, 21.01.2015, 23:35 | Сообщение # 283 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Что есть HN3 ? Я с таким не сталкивался...
HN3 - это азотистоводородная (азидоводородная) кислота.
H-N=N+=N- <----> H-N--N+≡N
Азид - анион, в некотором смысле - аналог гапогена.
|
|
| |
| |
| |
| Egor | Дата: Четверг, 22.01.2015, 00:21 | Сообщение # 284 |
|
Группа: Пользователи
Сообщений: 267
| Спасибо!
Есть у нас тиофен. На 4 атома углерода приходится 6π-электронов, поэтому он является πе-избыточным.
Есть у нас пиридин. На 6 атомов углерода приходится 8п-электронов (6п-электронов лично пиридина и пара электронов от азота).
Он является пе-недостаточным.
Чего я не понимаю?
Сообщение отредактировал Egor - Четверг, 22.01.2015, 01:27 |
|
| |
| |
| |
| Egor | Дата: Четверг, 22.01.2015, 01:12 | Сообщение # 285 |
|
Группа: Пользователи
Сообщений: 267
| Есть смесь бензола и тиофена, бромируем. Сначала бромируется тиофен. Из этого делаем вывод, что он более реакционно способный.
За счет чего проявляется эта реакционная способность тиофена?
|
|
| |
| |
| |