|
Одновалентная медь
|
|
| Miriada | Дата: Пятница, 01.04.2016, 21:26 | Сообщение # 16 |

Группа: Пользователи
Сообщений: 699
| Под "лохматостью" Вы имеете в виду стерические затруднения? 
|
|
| |
| |
| |
| Ефим | Дата: Пятница, 01.04.2016, 21:29 | Сообщение # 17 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) Под "лохматостью" Вы имеете в виду стерические затруднения?
Именно! 
|
|
| |
| |
| |
| Miriada | Дата: Пятница, 01.04.2016, 21:32 | Сообщение # 18 |

Группа: Пользователи
Сообщений: 699
| А вообще Вы абсолютно правы на счёт изображения второго интермедиата. Ведь даже судить о влиянии различных факторов на окислительную циклизацию гораздо проще, имея более подробное и правильное изображение структуры интермедиата (металлокомплекса).
|
|
| |
| |
| |
| Miriada | Дата: Пятница, 01.04.2016, 21:35 | Сообщение # 19 |

Группа: Пользователи
Сообщений: 699
| Выходит, что и молекулы именно полярных растворителей также могут стабилизировать заряженный металлокомплекс?
|
|
| |
| |
| |
| Miriada | Дата: Пятница, 01.04.2016, 21:38 | Сообщение # 20 |

Группа: Пользователи
Сообщений: 699
| А такое изображение тоже не является всё-таки корректным?
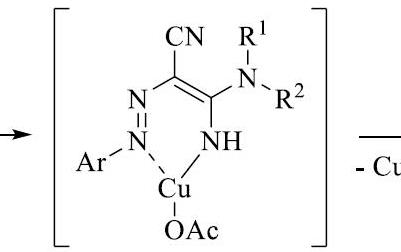
|
|
| |
| |
| |
| Ефим | Дата: Пятница, 01.04.2016, 21:48 | Сообщение # 21 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) А вообще Вы абсолютно правы на счёт изображения второго интермедиата. Ведь даже судить о влиянии различных факторов на окислительную циклизацию гораздо проще, имея более подробное и правильное изображение структуры интермедиата (металлокомплекса).
Вот в этом - основная проблема. Чем дольше я смотрю на эти картинки (в том числе - свои), тем меньше они мне нравятся. Дело в том, что интермедиат-2 в том виде, в котором я его нарисовал - это вообще не комплекс, это полноценная медная соль вполне себе ковалентной структуры. Это не есть хорошо, это ОЧЕНЬ сомнительно. Двух(простименягосподи)валентная медь в таком окружении - это жуткий артефакт. Для любого металлокомплекса характерно насыщение координационной сферы металла. Медь(II) тут должна быть четырёхкоординированной. Меди(I) дозволено быть двухкоординированной.
P.S. У меня этот вопрос в разработке, но в пятницу вечером я нет рискну рисовать структуры. Как бы рука не дрогнула :D
Прокрастинируем эту тему до завтра.
|
|
| |
| |
| |
| Ефим | Дата: Пятница, 01.04.2016, 21:52 | Сообщение # 22 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) А такое изображение тоже не является всё-таки корректным?
Оно намного лучше! Вот только откуда OAc взялся, которого раньше не было :)
Такое изображение куда ближе к каноническим изображениям металлокомплексов.
Всё пошёл спать. Утро вечером мудренее. Или как там?
Сообщение отредактировал Ефим - Пятница, 01.04.2016, 21:56 |
|
| |
| |
| |
| Miriada | Дата: Пятница, 01.04.2016, 21:59 | Сообщение # 23 |

Группа: Пользователи
Сообщений: 699
| Это просто изображение от реакции , катализируемой ацетатом меди, а не хлоридом. 
|
|
| |
| |
| |
| Miriada | Дата: Суббота, 02.04.2016, 10:36 | Сообщение # 24 |

Группа: Пользователи
Сообщений: 699
| Если рассматривать природу аминов относительно влияния именно на окислительную циклизацию, то имеет место тот же ряд а > в > г > д > б > е ?
Вообще, всё, что увеличивает стабильность интермедиата на второй стадии, в частности электронодонорные заместители, будет увеличивать скорость образования триазола...Но я так рассуждаю, исходя всё-таки из тех структур, которые Вы приводили в самом начале.
|
|
| |
| |
| |
| Ефим | Дата: Суббота, 02.04.2016, 18:48 | Сообщение # 25 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) Если рассматривать природу аминов относительно влияния именно на окислительную циклизацию, то имеет место тот же ряд а > в > г > д > б > е ?
Этот ряд отражает исключительно нуклеофильность аминов в реакции присоединения. Конкретная реакция окислительной циклизации к нуклеофильности аминов не имеет никакого отношения, и регулируется совсем другими эффектами. Тут вы пытаетесь "натянуть сову на глобус" 
|
|
| |
| |
| |
| Ефим | Дата: Суббота, 02.04.2016, 19:00 | Сообщение # 26 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) Вообще, всё, что увеличивает стабильность интермедиата на второй стадии, в частности электронодонорные заместители, будет увеличивать скорость образования триазола...Но я так рассуждаю, исходя всё-таки из тех структур, которые Вы приводили в самом начале.
Это не факт. Образование комплекса - это одна реакция, его окисление - другая. Интермедиат - это не переходное состояние, более стабильный интермедиат может оказаться и более стабильным к окислению. Надо учитывать механизм именно окисления, а стабильность интермедиата - это вопрос второго плана.
Мне в этой реакции до сих пор неясно - имеет ли место ред-окс катализ (то есть непосредственным окислителем является медь, окисляющаяся впоследствии кислородом), или окисляется сам металлокомплекс, непосредственно кислородом, а медь выполняет роль координатора, понижающего энергию переходного состояния. Тот факт, что реакция катализируется как двух-, так и одновалентной медью указывает на второй вариант. Но тут ещё надо разобраться - что имеется в виду под словом "катализирует". Одновалентная медь может превращаться в двухвалентную, включаясь в каталитический цикл, но фактически она в цикле не будет присутствовать. Тогда и первый вариант имеет право на существование.
Но в любом случае, рассматривать здесь "эффекты заместителей" (в плане донор-акцептор) нет абсолютно никаких оснований.
|
|
| |
| |
| |
| Miriada | Дата: Суббота, 02.04.2016, 21:03 | Сообщение # 27 |

Группа: Пользователи
Сообщений: 699
| Выходит, прежде чем пытаться объяснить влияние различных факторов на протекание той или иной реакции, необходимо однозначно установить механизм этой реакции. Но, с другой стороны, чтобы установить механизм, мы изучаем влияние различных факторов и пытаемся тем или иным образом трактовать получаемые результаты, опираясь на общеизвестные теории, закономерности. Замкнутый круг получается...Или я что-то не понимаю?
|
|
| |
| |
| |
| Ефим | Дата: Воскресенье, 03.04.2016, 19:49 | Сообщение # 28 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Miriada (  ) Выходит, прежде чем пытаться объяснить влияние различных факторов на протекание той или иной реакции, необходимо однозначно установить механизм этой реакции. Но, с другой стороны, чтобы установить механизм, мы изучаем влияние различных факторов и пытаемся тем или иным образом трактовать получаемые результаты, опираясь на общеизвестные теории, закономерности. Замкнутый круг получается...Или я что-то не понимаю?
В самом общем случае мы постулируем некий механизм, на наш взгляд - наиболее вероятный, и смотрим, как на реакционную способность в этом случае должны влиять заместители, и как они влияют реально. Если наблюдаем хорошую корреляцию - ставим плюсик, и считаем этот механизм возможным.
То есть - первичным является именно предположение о механизме. Его нельзя "установить", можно только доказательно предложить. И если предложенный механизм доказан наблюдаемыми эффектами - его можно считать "установленным" (до первого наблюдения, ему противоречащего, после чего - "на колу мочало, начинай сначала"  ). ).
В данном, конкретном случае, у нас просто нет данных, позволяющих выбрать из серии возможных механизмов наиболее вероятный. Приходится руководствоваться только "общими соображениями" и художественным вкусом при рисовании структур :)
Тут мне вспомнилась история из собственной практики.
Была такая тема - реакция хлорацетонитрила (Cl-CH2-CN) с нафталином в присутствии соединений железа. Судили-рядили - вроде обычная реакция Фриделя-Крафтса, но, оказалось, что она катализируется бромом. То есть (в условиях реакции) - бромистым водородом. Напрашивалась реакция по типу Финкельштейна, с заменой хлора на бром в исходном хлорацетонитриле и быстрая реакция уже бромацетонитрила с нафталином. Изготовил я бромацетонитрил, проверил - да, так оно и есть. Но! В реакции Фриделя-Крафтса бромиды менее активны, чем хлориды, то есть, факт катализа бромом опровергает предположение о механизме Фриделя-Крафтса. Почесав репу остановились на радикальном присоединении (нафталин к нему весьма склонен), где нашлось место железу (переменная валентность) и брому (лёгкий гоморазрыв C-Br связи). В результате в качестве катализатора предложили бромистое железо(II), кое и было с успехом использовано.
Первичным является представление о механизме, к которому примериваются экспериментальные факты.
Сообщение отредактировал Ефим - Воскресенье, 03.04.2016, 20:03 |
|
| |
| |
| |
| Miriada | Дата: Воскресенье, 10.04.2016, 12:45 | Сообщение # 29 |

Группа: Пользователи
Сообщений: 699
| Ефим, можно Вам задать вопрос не совсем по теме, но он касается катализа?
Не могу понять принципиальное отличие кислотного катализа специфического от общего.
Правильно ли я понимаю, что отличие состоит лишь в том, что в специфическом протонирование осуществляется именно ионом гидроксония, а в общем вообще любыми кислотами Бренстеда?
То есть специфический кислотный катализ наблюдается только в том случае, если pKa протонированной формы реагента меньше (по абсолютному значению), чем pKa иона гидроксония? Но у некоторых кислот pKa ещё меньше, они тоже могут участвовать в специфическом катализе...Кажется, я слегка запуталась. Не могли бы Вы помочь разобраться?
|
|
| |
| |
| |
| Miriada | Дата: Воскресенье, 10.04.2016, 14:41 | Сообщение # 30 |

Группа: Пользователи
Сообщений: 699
| И то же самое с основным катализом. Почему альдольная конденсация, например, является примером именно специфического основного катализа?
|
|
| |
| |
| |