| Miriada | Дата: Суббота, 21.09.2013, 15:28 | Сообщение # 1 |

Группа: Пользователи
Сообщений: 699
| Здравствуйте! Не могли бы Вы проверить несколько несложных задач по органической химии?
Задача 1.
Найдите эмпирическую и молекулярную формулы соединения, если известны его процентный состав и молекулярный вес.
ДАНО:
С- 34,6
H - 3,9
O - 61.5
M= 104
РЕШЕНИЕ:
n( C)=3
n(H)=4
n(O)=4
Эмпирическая формула С3H4O4
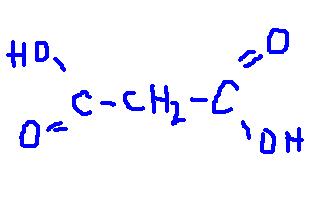
Задача 2.
При нагревании 1-бромпропана с водной щёлочью выделилось 79,8 г пропанола. Сколько 1-бромпропана было взято,если реакция прошла с 53% выходом?
ДАНО:
m прак. ( C3H7OH)=79,8 г
W=53%
Найти : m прак. (C3H7Br)
РЕШЕНИЕ
C3H7Br+NaOH=C3H7OH+NaBr
Сначала находим теоретическую массу C3H7OH : m теор. ( C3H7OH)=79,8/0,55=150,57 г
Теперь найдём теоретическое количество вещества для продукта C3H7OH: n теор.( C3H7OH) = 150,57/60=2,5 моль
Тогда по уравнению n теор. ( C3H7Br) =2,5 моль
Следовательно, m теор. ( C3H7Br)=307,5 г
И тогда m прак. ( C3H7Br)=W * m теор. ( C3H7Br)=307,5*0,53=163 г
Ответ: 163 г.
Задача 3
Предскажите соотношение изомерных продуктов монобромирования углеводородов, учитывая, что скорости замещения водорода при первичном, вторичном и третичном атомах углерода в алканах относятся, как 1:100:200.
ДАНО: 3,3-диметилгексан
РЕШЕНИЕ: ( думаю, что нужно рассуждать след. образом)
Количество первичных атомов углерода - 4, вторичных - 3, третичных нет.
Исходя из условия, можно написать, что константы скорости относятся, как k1:k2:k3=1:100:200
И отсюда мы можем посчитать относительное количество продуктов:
В случае замещения водорода у первичных атомов: (4*1)/(4*1+3*100)=0,013 или 1,3 %. Тогда относительное количество продуктов замещения у вторичных углеродов 100%-1,3%=98,7%, т.е. соотношение будет 1,3:98,7
Задача 4
Какие углеводороды образуются при действии металлического натрия на смесь следующих галогенпроизводных? Напишите уравнения реакций и назовите полученные соединения.
Исходная смесь: хлористый метил и 1-хлор-3-метилбутан.
2 CH3Cl+2Na=H3C-CH3 +2NaCl
2 H2C(Cl)- CH2-CH(CH3)-CH3+2Na = H3C-CH(CH3)-CH2-CH2-CH2-CH2-CH2(CH3)-CH3 ( 2, 7 - диметилоктан) + 2NaCl
|
|
| |
| |
| |
| Ефим | Дата: Суббота, 21.09.2013, 16:22 | Сообщение # 2 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата (Miriada) Задача 2. При нагревании 1-бромпропана с водной щёлочью выделилось 79,8 г пропанола. Сколько 1-бромпропана было взято,если реакция прошла с 53% выходом?
ДАНО:
m прак. ( C3H7OH)=79,8 г
W=53%
Найти : m прак. (C3H7Br)
РЕШЕНИЕ
C3H7Br+NaOH=C3H7OH+NaBr
Сначала находим теоретическую массу C3H7OH : m теор. ( C3H7OH)=79,8/0,55=150,57 г
Теперь найдём теоретическое количество вещества для продукта C3H7OH: n теор.( C3H7OH) = 150,57/60=2,5 моль
Тогда по уравнению n теор. ( C3H7Br) =2,5 моль
Следовательно, m теор. ( C3H7Br)=307,5 г
И тогда m прак. ( C3H7Br)=W * m теор. ( C3H7Br)=307,5*0,53=163 г
Ответ: 163 г.
Тут у Вас ошибка в рассуждениях. "Выход 53%" означает, что спирта получилось меньше, чем было взято галогенида. А это значит, что практическое количество взятого бромпропана будет равно теоретическому количеству спирта, то есть 2.5 моль, соответственно масса взятого бромпропана 307.5 г.
Цитата (Miriada) Задача 3 Предскажите соотношение изомерных продуктов монобромирования углеводородов, учитывая, что скорости замещения водорода при первичном, вторичном и третичном атомах углерода в алканах относятся, как 1:100:200.
ДАНО: 3,3-диметилгексан
РЕШЕНИЕ: ( думаю, что нужно рассуждать след. образом)
Количество первичных атомов углерода - 4, вторичных - 3, третичных нет.
Исходя из условия, можно написать, что константы скорости относятся, как k1:k2:k3=1:100:200
И отсюда мы можем посчитать относительное количество продуктов:
В случае замещения водорода у первичных атомов: (4*1)/(4*1+3*100)=0,013 или 1,3 %. Тогда относительное количество продуктов замещения у вторичных углеродов 100%-1,3%=98,7%, т.е. соотношение будет 1,3:98,7
А здесь Вы не учли количество атомов водорода при каждом атоме. Отношение скорости замещения первичного атома водорода к скорости замещения вторичного равно 1:100, но количество атомов водорода у атомов углерода разного типа - разное, и это надо учитывать! При 4-х первичных углеродах имеем 12 атомов Н, при 3-х вторичных - 6 атомов Н.
В задании сказано "предскажите соотношение изомерных продуктов", а не просто отношение первичный/вторичный.
3,3-диметилгексан образует 6 монобромпроизводных, 3 первичных и 3 вторичных:
1. Br-CH2-CH2-C(CH3)2-CH2-CH2-CH3 (3)
2. CH3-CH2-C(CH3)2-CH2-CH2-CH2Br (3)
3. CH3-CH2-C(CH2Br)(CH3)-CH2-CH2-CH3 (6)
4. CH3-CHBr-C(CH3)2-CH2-CH2-CH3 (2)
5. CH3-CH2-C(CH3)2-CHBr-CH2-CH3 (2)
6. CH3-CH2-C(CH3)2-CH2-CHBr-CH3 (2)
Относительная вероятность образования конкретного изомера равна количеству атомов водорода у реакционного атома углерода (даны в скобках). У выделенного изомера (3) это число равно 6-ти, поскольку замещение в обоих метильных группах приводит к одному и тому же изомеру.
А теперь можем вычислить содержание всех изомеров:
(3*1)/(12*1+6*100)= 0.5% для 1 и 2
(6*1)/(12*1+6*100)= 1.0% для 3
(2*100)/(12*1+6*100)= 32.7% для 4, 5 и 6
Цитата (Miriada) Задача 4 Какие углеводороды образуются при действии металлического натрия на смесь следующих галогенпроизводных? Напишите уравнения реакций и назовите полученные соединения.
Исходная смесь: хлористый метил и 1-хлор-3-метилбутан.
2 CH3Cl+2Na=H3C-CH3 +2NaCl
2 H2C(Cl)- CH2-CH(CH3)-CH3+2Na = H3C-CH(CH3)-CH2-CH2-CH2-CH2-CH2(CH3)-CH3 ( 2, 7 - диметилоктан) + 2NaCl
CH3Cl + ClCH2-CH2-CH(CH3)-CH3 --(2Na)-->
Сообщение отредактировал Ефим - Суббота, 21.09.2013, 16:24 |
|
| |
| |
| |
| Miriada | Дата: Суббота, 21.09.2013, 17:37 | Сообщение # 3 |

Группа: Пользователи
Сообщений: 699
| Спасибо Вам большое, Ефим! Но я вот не могу понять ход рассуждений во второй задаче.
Цитата "Выход 53%" означает, что спирта получилось меньше, чем было взято галогенида.
Эта часть мне понятна. А дальше, извините, но я не могу уловить ваш ход мыслей. Ведь когда мы считаем что-либо по пропорциям ( по уравнению), то мы же получаем теоретические значения. Или нет?Добавлено (21.09.2013, 17:37)
---------------------------------------------
Или так : если бы 2,5 моль C3H7Br было теоретическим количеством вещества, то практическое количество вещества C3H7Br было бы меньше. Но из меньшего количества вещества не может получиться большее. Верно?
|
|
| |
| |
| |
| Ефим | Дата: Суббота, 21.09.2013, 20:08 | Сообщение # 4 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата (Miriada) Или так : если бы 2,5 моль C3H7Br было теоретическим количеством вещества, то практическое количество вещества C3H7Br было бы меньше. Но из меньшего количества вещества не может получиться большее. Верно?
Понятия "теретическое" и "практическое" количество относятся только к продукту реакции. Мы берём в реакцию Х грамм бромпропана (это данность), и рассчитываем получить X/M(бромпропан)*M(пропанол) граммов спирта. Это - теоретический выход. Проводим реакцию, и получаем всего 53% от рассчётной массы спирта, то есть X/M(бромпропан)*M(пропанол)*0.53 граммов. Это - практический выход. Отсюда и находим X:
X/M(бромпропан)*M(пропанол)*0.53 = 79.8
X = 79.8*M(пропанол)/M(бромпропан)/0.53 = 79.8/60*123/0.53 = 308.7 г
И это число - оно не практическое, и не теоретическое - это данность, столько взяли исходного вещества. Сколько взяли, столько и взяли. Точка. 
Или, другими словами: при 53%-м выходе мы получили 79.8 г спирта. Очевидно, что при 100%-м выходе мы получили бы 79.8/0.53 = 150.5 г спирта. Но на это количество требуется 150.5/60*123 = 308.5 г бромпропана. Столько и было взято.
Сообщение отредактировал Ефим - Суббота, 21.09.2013, 20:13 |
|
| |
| |
| |
| Miriada | Дата: Воскресенье, 22.09.2013, 09:56 | Сообщение # 5 |

Группа: Пользователи
Сообщений: 699
| СПАСИБО БОЛЬШОЕ!!! Всё теперь стало ясно  . .
|
|
| |
| |
| |