|
Органическая химия. Вопросы.
|
|
| Ефим | Дата: Понедельник, 24.11.2014, 22:10 | Сообщение # 196 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) У диметилпропионового альдегида вообще нет водорода в α-положении. Значит, это карбонильная компонента. СН-кислотой, т.е. метиленовой компонентой, будет ацетон.
При действии основания ацетон отщепляет протон от α-СН-кислотного центра и превращается в карбанион.
H2C--CO-CH3 <----> CH3-CO--CH3.
Он же в свою очередь, являясь сильным нуклеофилом, присоединяется к молекуле диметилпропионового альдегида.
(CH3)CHO + H2C--CO-CH3 -----> (CH3)C-C(H)(O-)-CH2-CO-CH3 ----H2O-----> (CH3)C-C(H)(OH)-CH2-CO-CH3 + OH-.
Получили альдоль. Но у нас среда кислая, будет продукт кротоновой конденсации.
(CH3)C-C(H)(OH)-CH2-CO-CH3 ---Н+--->
У нас этот углерод уже 4-валентный, если будет замыкаться двойная связь, то получится, что валентность уже 5.
Где я ошибся?
А откуда основание, если среда - кислая? Альдольная конденсация катализируется не только основаниями, но и кислотами (хотя в этом случае скорость реакции существенно ниже). При кислотном катализе атакующая частица - электрофил, образующийся при протонировании карбонильной компоненты:
(CH3)3C-CH=O --(H+)--> (CH3)3C-C+H-OH
Метиленовая компонента реагирует в виде енола (енолизация катализируется кислотой):
СH3-CO-CH3 --(H+)--> CH3-C+(OH)-CH3 --(-H+)--> CH3-C(OH)=CH2
Тут стоит отметить, что кислота не увеличивает равновесное содержание енола, но ускоряет установление равновесия. Сам по себе процесс енолизации - весьма медленный.
Енол подвергается электрофильной атаке по двойной связи:
CH3-C(OH)=CH2 + (CH3)3C-C+H-OH ----> CH3-C+(OH)-CH2-CH(OH)-C(CH3)3 --(-H+)--> CH3-CO-CH2-CH(OH)-C(CH3)3
А что касается стадии кротонизации, то углерод не тот выбран. Водород-то отщепляется от углерода в альфа-положении к карбонилу:
CH3-CO-CH2-CH(OH)-C(CH3)3 --(H+, -H2O)--> CH3-CO-CH=CH-C(CH3)3
Что интересно, если кетон (метиленовая компонента) несимметричный, то щелочной и кислотный катализ могут приводить к разным продуктам.
Сообщение отредактировал Ефим - Понедельник, 24.11.2014, 22:13 |
|
| |
| |
| |
| денис1 | Дата: Суббота, 29.11.2014, 17:04 | Сообщение # 197 |

Группа: Пользователи
Сообщений: 1146
| Цитата Ефим (  ) Крутится в голове, что тройная связь менее доступна для электрофильной атаки. А вот откуда это - надо поискать.
Когда найдёте, сообщите мне. А то парадокс какой-то получается. То по двойной, то по тройной связи...
За ответы спасибо!
|
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |
| Ефим | Дата: Суббота, 29.11.2014, 20:46 | Сообщение # 198 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата денис1 (  ) Когда найдёте, сообщите мне. А то парадокс какой-то получается. То по двойной, то по тройной связи...
Вот, нашёл. У своего любимого Физера (1-й том):

Кстати, о каком парадоксе идет речь?
Сообщение отредактировал Ефим - Суббота, 29.11.2014, 20:50 |
|
| |
| |
| |
| денис1 | Дата: Воскресенье, 30.11.2014, 00:06 | Сообщение # 199 |

Группа: Пользователи
Сообщений: 1146
| Цитата Ефим (  ) Кстати, о каком парадоксе идет речь?
не парадокс это, так просто назвал то, что к сопряжённым енинам присоединение идёт по тройной связи, хотя она менее подвержена электрофильной атаке. Почему это происходит?
|
|
|
Е.В.Базаров: "Порядочный химик в двадцать раз полезнее всякого поэта". |
| |
| |
| Ефим | Дата: Воскресенье, 30.11.2014, 19:12 | Сообщение # 200 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата денис1 (  ) не парадокс это, так просто назвал то, что к сопряжённым енинам присоединение идёт по тройной связи, хотя она менее подвержена электрофильной атаке. Почему это происходит?
А где упоминается этот факт? Это интересно.
В сопряжённом енине тройная связь будет акцептором:
CH2=CH-C≡CH <----> CH2+-CH=C=CH-
Хотя может быть и донором:
CH2=CH-C≡CH <----> CH2--CH=C=CH+
Но это явно менее вероятно.
Если рассматривать направление протонирования без учёта статических эффектов, то
CH2=CH-C≡CH <--(H+)--> CH3-CH+-C≡CH <----> CH3-CH=C=CH+
CH2=CH-C≡CH <--(H+)--> CH2=CH-C+=CH2 <----> CH2+-CH=C=CH2
присоединение по двойной связи так же выглядит предпочтительнее.
Правда, тут вопрос возникает о судьбе возникающего аллена. Если напрочь отказаться от алленовой структуры, то факт сопряжения вообще становится ни на что не влияющим, в этом случае можно сравнивать только два катиона:
CH3-CH+-C≡CH
CH2=CH-C+=CH2
Первый дестабилизирован сигма-акцептором (углеродом sp), второй возникает на углероде sp2, что тоже не стабилизирует его. Если факт преимущественного 1,2-присоединения по тройной связи в сопряжённом енине имеет место, значит первый катион дестабилизирован сильнее, а сопряжённые алленовые структуры не играют роли в виду ещё более высокой энергии.
|
|
| |
| |
| |
| Egor | Дата: Понедельник, 01.12.2014, 19:52 | Сообщение # 201 |
|
Группа: Пользователи
Сообщений: 267
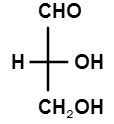
| Есть у нас D-глицериновый альдегид. Это R-изомер.
Почему? Падение старшинства должно быть по часовой стрелке. Но ОН старше СНО; не получается падения старшинства.
|
|
| |
| |
| |
| Grey | Дата: Понедельник, 01.12.2014, 21:18 | Сообщение # 202 |
|
Группа: Пользователи
Сообщений: 133
| Цитата Egor (  ) Есть у нас D-глицериновый альдегид. Это R-изомер. Почему? Падение старшинства должно быть по часовой стрелке. Но ОН старше СНО; не получается падения старшинства.
Возможно из-за старшинства заместителей, содержащих кратные связи. Формильную группу следует считать более старшей, чем гидроксиметильную.
(см. В.Ф.Травень Органическая химия том 1)
|
|
| |
| |
| |
| Egor | Дата: Понедельник, 01.12.2014, 22:17 | Сообщение # 203 |
|
Группа: Пользователи
Сообщений: 267
| На лекции был дан следующий ряд старшинства OH>CHO>CH2OH>H.
Возник еще второй вопрос.
Кето-енольная таутомерия D-фруктозы. Формулу ендиола пропустил. Что означает ~ ?
То, что гидроксил может находиться "справа и слева"?
|
|
| |
| |
| |
| Ефим | Дата: Понедельник, 01.12.2014, 22:25 | Сообщение # 204 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Есть у нас D-глицериновый альдегид. Это R-изомер. Почему? Падение старшинства должно быть по часовой стрелке. Но ОН старше СНО; не получается падения старшинства.
С проекцией Фишера нельзя так обращаться. Дело в том, что в проекции Фишера "горизонтальные" связи направлены к наблюдателю. В данном случае это связь C-H (водород - самый младший) А по правилу RS-номенклатуры связь с самым младшим заместителем должна быть "от наблюдателя". Если провести эту операцию с данной проекцией Фишера, то можно убедиться, что это всё-таки R-конфигурация:

Существует простое правило для определения RS-конфигурации структуры в проекции Фишера:
"Если самый младший заместитель расположен по горизонтали, то направление обхода оставшихся заместителей по правилу RS-номенклатуры даёт противоположную конфигурацию."
Цитата Grey (  ) Возможно из-за старшинства заместителей, содержащих кратные связи. Формильную группу следует считать более старшей, чем гидроксиметильную.
Формильная группа действительно старше, чем гидроксиметильная, но проблема не в этом.
Сообщение отредактировал Ефим - Понедельник, 01.12.2014, 22:36 |
|
| |
| |
| |
| Egor | Дата: Вторник, 02.12.2014, 19:54 | Сообщение # 205 |
|
Группа: Пользователи
Сообщений: 267
| Цитата Лёгкость лактонизации γ- и δ-гидроксикислот объясняет повышенной т/д устойчивостью пяти- и шестичленных циклических соединений.
Если возьмем 4-гидроксимасляную кислоту, то получим γ-бутиролактон, но это же 4-членный цикл. Почему мы его можем получить?
кажется, я по фигне запарился.
|
|
| |
| |
| |
| Ефим | Дата: Вторник, 02.12.2014, 21:14 | Сообщение # 206 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Кето-енольная таутомерия D-фруктозы. Формулу ендиола пропустил. Что означает ~ ? То, что гидроксил может находиться "справа и слева"?
Справа что-то невнятное нарисовано. Должно быть это?
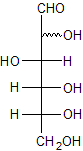
Волнистой линией обычно обозначают связь в том случае, если конфигурация равновероятна или неопределённа. В данном случае это означает, что получаются оба стереоизомера (глюкоза и манноза), а их относительное количество от условий реакции зависит. В общем получается равновесная смесь, содержащая смесь глюкозы, фруктозы и маннозы в неравных количествах
Цитата Egor (  ) Если возьмем 4-гидроксимасляную кислоту, то получим γ-бутиролактон, но это же 4-членный цикл. Почему мы его можем получить?
Не-а, пятичленный, аднака 
Цитата Egor (  ) кажется, я по фигне запарился.
Отдыхать надо, отвлекаться. Химия никуда не денется 
|
|
| |
| |
| |
| Egor | Дата: Вторник, 02.12.2014, 21:21 | Сообщение # 207 |
|
Группа: Пользователи
Сообщений: 267
| Цитата Не-а, пятичленный, аднака
Через какую программы Вы изображаете формулы - ChemSketch?
Я вчера скачал, получилось составить только линейные структуры, а как проекцию Фишера нарисовать - не нашел.
Куда нажимать там надо 
|
|
| |
| |
| |
| Ефим | Дата: Вторник, 02.12.2014, 22:37 | Сообщение # 208 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) Через какую программы Вы изображаете формулы - ChemSketch? Я вчера скачал, получилось составить только линейные структуры, а как проекцию Фишера нарисовать - не нашел.
Куда нажимать там надо
Да, ChemSketch. Там нарисовать можно всё, что угодно, причём разными способами.
"Проекции Фишера" - это, по сути - те же обычные структуры, просто углы между связями - прямые. Этого можно добиться тремя способами:
1) Рисовать обычную "угловую" структуру, а потом вручную, мышкой править углы, таская атомы. Очень нудное занятие, и получается не красиво.
2) Использовать тройную CC-связь для построения линейной структуры, где боковые атомы автоматом ставятся под прямым углом:
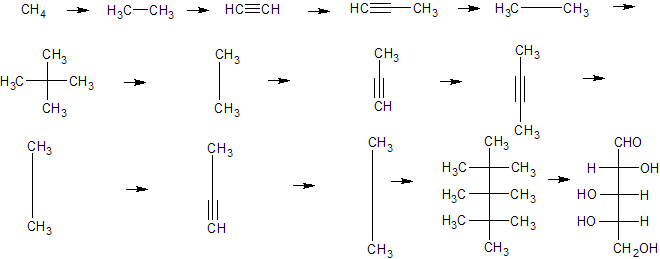
Это намного быстрее и не утомительно - сидишь, левой кнопой клацаешь, а оно само строится.
3) Воспользоваться готовыми образцами (Меню "Templates" - "Template Window" - "Carbohydrates") Это быстрее всего.
Вообще - там очень много возможностей, скрытых в менюшках и панелях инструментов. Рассказать обо всём - это надо книжку написать.
|
|
| |
| |
| |
| Egor | Дата: Среда, 03.12.2014, 01:22 | Сообщение # 209 |
|
Группа: Пользователи
Сообщений: 267
| Ага, разобрался. Спасибо!
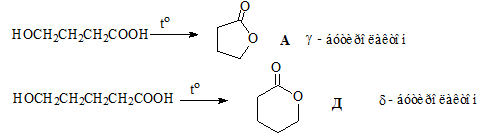
В задачнике соединение А называется γ-бутиролактон, а Д - δ-бутиролактон.
Почему везде "бутиро"? Бутираты - соли масляной кислоты. Почему так называется вещество А - понятно.
Д - это же валериановая кислота только с гидроксилом.
|
|
| |
| |
| |
| Ефим | Дата: Среда, 03.12.2014, 09:44 | Сообщение # 210 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Egor (  ) задачнике соединение А называется γ-бутиролактон, а Д - δ-бутиролактон. Почему везде "бутиро"? Бутираты - соли масляной кислоты. Почему так называется вещество А - понятно.
Д - это же валериановая кислота только с гидроксилом.
Это ошибка. Соединение D - это δ-валеролактон.
|
|
| |
| |
| |