|
переход от проекции Ньюмена к проекции Фишера
|
|
| Werossa | Дата: Среда, 29.01.2014, 17:49 | Сообщение # 1 |

Группа: Пользователи
Сообщений: 282
| Добрый день, уважаемые профессионалы-химики!
Прошу Вашей помощи в освоении стереохимии органических соединений.
Цель упражнения - перейти от проекции Ньюмена к проекции Фишера и изобразить соединение в молекулярном виде.
Проекция Ньюмена:
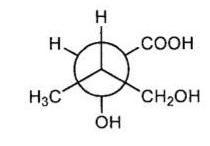
Ход мыслей:
1. Определила, что это заторможенная конфигурация.
2. В долгом и мучительном познавательном процессе родилась проекция Фишера:
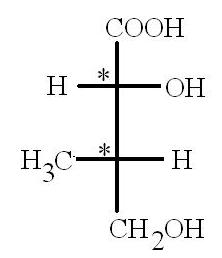
Получается - два асимметричных атома углерода.
Название - 2,4-диокси-3-метилбутановая кислота.
Перспективная проекция (для тренировки воображения):
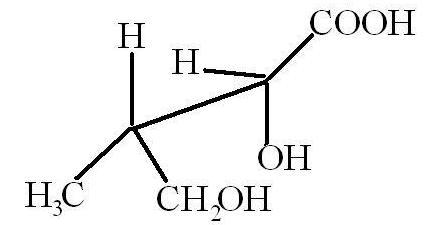
3. Изначально не поняла в задании - что значит "изобразить в молекулярном виде". Подскажите, пожалуйста - это обычная плоская структурная формула?
Заранее признательна за уделенное моему вопросу внимание!
Сообщение отредактировал Werossa - Среда, 29.01.2014, 17:51 |
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |
| Ефим | Дата: Среда, 29.01.2014, 20:54 | Сообщение # 2 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Werossa (  ) перейти от проекции Ньюмена к проекции Фишера
Не та конфигурация у Вас получилась в проекции Фишера.
Первый шаг - переходим от проекции Ньюмена к перспективной. Тут всё правильно. А дальше - учтём тот факт, что в проекции Фишера горизонтальные связи направлены "вверх" (над плоскостью рисунка), а вертикальные - вниз. Поэтому повернём верхний узел перспективной проекции так, чтобы COOH группа была внизу, и нижний узел - так, чтобы CH2OH группа смотрела вниз. После этого положим эту проекцию на лист бумаги и распрямим все углы - получится проекция Фишера:
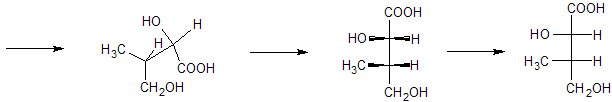
Обратная операция снова даст нам перспективную проекцию.
Цитата Werossa (  ) Изначально не поняла в задании - что значит "изобразить в молекулярном виде". Подскажите, пожалуйста - это обычная плоская структурная формула?
Вот тут я не знаю - что такое "молекулярный вид". Впервые сталкиваюсь с таким пожеланием 
|
|
| |
| |
| |
| Werossa | Дата: Четверг, 30.01.2014, 00:59 | Сообщение # 3 |

Группа: Пользователи
Сообщений: 282
| Цитата Ефим (  ) Первый шаг - переходим от проекции Ньюмена к перспективной. Тут всё правильно. А дальше - учтём тот факт, что в проекции Фишера горизонтальные связи направлены "вверх" (над плоскостью рисунка), а вертикальные - вниз. Поэтому повернём верхний узел перспективной проекции так, чтобы COOH группа была внизу, и нижний узел - так, чтобы CH2OH группа смотрела вниз. После этого положим эту проекцию на лист бумаги и распрямим все углы - получится проекция Фишера: 
|
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |
| Werossa | Дата: Четверг, 30.01.2014, 19:00 | Сообщение # 4 |

Группа: Пользователи
Сообщений: 282
| В продолжение темы по стереоизомерам органических соединений разбираю стереоизомерию аминокислот.
Посмотрите, пожалуйста, свои опытным взглядом, уважаемые профессионалы, боюсь ошибиться в таком тонком деле...
Приведите структуру ( R )-валина, (S)-аспарагиновой кислоты, (S)-тирозинaв виде проекционных формул Фишера. Дайте систематические названия этих аминокислотам и отнесите их к D- или L-рядам.Вот что получилось:

Буду очень благодарна, если не оставите без внимания мои чистосердечные попытки ПОНЯТЬ этот важный вопрос 
Сообщение отредактировал Werossa - Четверг, 30.01.2014, 19:01 |
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |
| Ефим | Дата: Четверг, 30.01.2014, 21:00 | Сообщение # 5 |

Группа: Супермодераторы
Сообщений: 1839
| В проекции Фишера обычно не рисуют оптически неактивные узлы (в данном случае - это концевые группы). В каждом из этих соединений только один асимметрический атом (С-2), а всё остальное - это заместители.
В определении конфигурации Вы ошиблись, увы, в двух случаях из трех. Первое соединение на картинке имеет S-конфигурацию, второе - R. Надо развернуть аминогруппы в другую сторону. Третье - правильно.
Отнесение к D-L ряду тоже наоборот будет. "R" - это "правая" форма, соответствует D-ряду (само его название от decstra - "правый" происходит), S - левому ряду.
|
|
| |
| |
| |
| Werossa | Дата: Пятница, 31.01.2014, 10:26 | Сообщение # 6 |

Группа: Пользователи
Сообщений: 282
| Цитата Ефим (  ) В проекции Фишера обычно не рисуют оптически неактивные узлы (в данном случае - это концевые группы). В каждом из этих соединений только один асимметрический атом (С-2), а всё остальное - это заместители. В определении конфигурации Вы ошиблись, увы, в двух случаях из трех. Первое соединение на картинке имеет S-конфигурацию, второе - R. Надо развернуть аминогруппы в другую сторону. Третье - правильно.
Отнесение к D-L ряду тоже наоборот будет. "R" - это "правая" форма, соответствует D-ряду (само его название от decstra - "правый" происходит), S - левому ряду.
Добавлено (31.01.2014, 10:26)
---------------------------------------------
Цитата Ефим (  ) Отнесение к D-L ряду тоже наоборот будет. "R" - это "правая" форма, соответствует D-ряду (само его название от decstra - "правый" происходит), S - левому ряду.
Сообщение отредактировал Werossa - Пятница, 31.01.2014, 10:28 |
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |
| korenev | Дата: Пятница, 31.01.2014, 12:25 | Сообщение # 7 |

Группа: Пользователи
Сообщений: 67
| Цитата Werossa (  ) Меня смутила фраза в учебнике, что D / L конфигурация НЕ ВСЕГДА совпадает с R / S соответственно
Сообщение отредактировал korenev - Пятница, 31.01.2014, 12:26 |
|
| |
| |
| |
| Werossa | Дата: Пятница, 31.01.2014, 20:11 | Сообщение # 8 |

Группа: Пользователи
Сообщений: 282
| Цитата korenev (  ) Правильно, не всегда, например L-цистеин принадлежит к R-ряду. Но в случае с цистеином так происходит из-за серы (скажем так, сера старше кислорода). В большинстве же случаев D это R, а L это S. Добавлено (31.01.2014, 20:11)
---------------------------------------------
Цитата Werossa (  ) Но в случае с цистеином так происходит из-за серы (скажем так, сера старше кислорода) |
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |
| Ефим | Дата: Пятница, 31.01.2014, 22:34 | Сообщение # 9 |

Группа: Супермодераторы
Сообщений: 1839
| Цитата Werossa (  ) Я понимаю, о чем Вы говорите... это как раз к вопросу о старшинстве заместителей. Тут имеется в виду привязка к номеру атома в ПСХЭ?
Именно.
D,L - номенклатура не связана со старшинством заместителей и основана на соотнесении абсолютной конфигурации вещества со стандартом (глицериновым альдегидом).
R,S-номенклатура - универсальна, не связана с эталоном и может быть формальным образом применена к любому веществу.
Отсюда и возникают расхождения. Если взять L-аланин, то в R,S - номенклатуре его конфигурация будет обозначаться как S. Если к нему же подвесить меркапто-группу (HS-CH2-CH(NH2)COOH), то с точки зрения D,L-номенклатуры ничего не изменится - ведь абсолютная конфигурация асимметрического центра сохранилась, поэтому полученный цистеин будет по-прежнему принадлежать к L-ряду. А вот с точки зрения формальной R,S-номенклатуры - конфигурация поменялась, поскольку сера старше кислорода. И цистеин, оставаясь членом L-ряда, обретает R-конфигурацию.
Тут надо в каждом конкретном случае оценивать - как соотносятся эти номенклатуры. Каюсь - я упустил из виду этот момент, когда отвечал 
Сообщение отредактировал Ефим - Пятница, 31.01.2014, 23:40 |
|
| |
| |
| |
| Werossa | Дата: Суббота, 01.02.2014, 01:30 | Сообщение # 10 |

Группа: Пользователи
Сообщений: 282
| Цитата Ефим (  ) D,L - номенклатура не связана со старшинством заместителей и основана на соотнесении абсолютной конфигурации вещества со стандартом (глицериновым альдегидом). R,S-номенклатура - универсальна, не связана с эталоном и может быть формальным образом применена к любому веществу.
Отсюда и возникают расхождения. Если взять L-аланин, то в R,S - номенклатуре его конфигурация будет обозначаться как S. Если к нему же подвесить меркапто-группу (HS-CH2-CH(NH2)COOH), то с точки зрения D,L-номенклатуры ничего не изменится - ведь абсолютная конфигурация асимметрического центра сохранилась, поэтому полученный цистеин будет по-прежнему принадлежать к L-ряду. А вот с точки зрения формальной R,S-номенклатуры - конфигурация поменялась, поскольку сера старше кислорода. И цистеин, оставаясь членом L-ряда, обретает R-конфигурацию.
Тут надо в каждом конкретном случае оценивать - как соотносятся эти номенклатуры.
Спасибо Вам огромное, Ефим! Вопросы по стереохимии для меня одни из самых сложных, поэтому очень признательна Вам за такое исчерпывающее разъяснение!!
|
|
|
Не стыдно не знать. Стыдно не хотеть знать. |
| |
| |